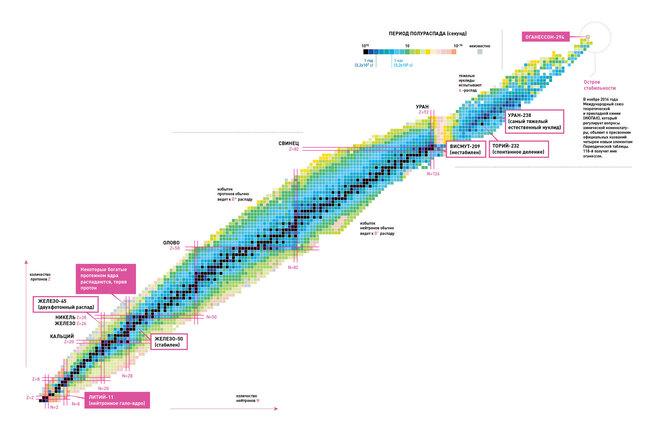
Limiete van die periodieke tabel van elemente. Waar is die gelukkige eiland van stabiliteit?
Het die periodieke tabel van elemente 'n "boonste" limiet - is daar dus 'n teoretiese atoomgetal vir 'n superswaar element wat onmoontlik sou wees om te bereik in die bekende fisiese wêreld? Die Russiese fisikus Yuri Oganesyan, na wie element 118 vernoem is, glo dat so 'n limiet moet bestaan.
Volgens Oganesyan, hoof van die Flerov-laboratorium by die Joint Institute for Nuclear Research (JINR) in Dubna, Rusland, is die bestaan van so 'n limiet die gevolg van relativistiese effekte. Soos die atoomgetal toeneem, neem die positiewe lading van die kern toe, en dit verhoog op sy beurt die spoed van elektrone rondom die kern, wat die spoedgrens van lig nader, verduidelik die fisikus in 'n onderhoud wat in die April-uitgawe van die joernaal gepubliseer is. . Nuwe Wetenskaplike. “Die elektrone naaste aan die kern in element 112 beweeg byvoorbeeld teen 7/10 die spoed van lig. As die buitenste elektrone die spoed van lig nader, sou dit die eienskappe van die atoom verander en die beginsels van die periodieke tabel oortree,” sê hy.
Die skep van nuwe superswaar elemente in fisika-laboratoriums is 'n vervelige taak. Wetenskaplikes moet met die grootste akkuraatheid die kragte van aantrekking en afstoting tussen elementêre deeltjies balanseer. Wat nodig is, is 'n "magiese" aantal protone en neutrone wat in die kern met die verlangde atoomgetal "aanmekaar vashou". Die proses self versnel die deeltjies tot 'n tiende van die spoed van lig. Daar is 'n klein, maar nie nul nie, kans op die vorming van 'n superswaar atoomkern van die vereiste getal. Dan is die taak van fisici om dit so vinnig moontlik af te koel en dit in die detektor te “vang” voordat dit verval. Hiervoor is dit egter nodig om die toepaslike "grondstowwe" te verkry - skaars, uiters duur isotope van elemente met die nodige neutronhulpbronne.
In wese, hoe swaarder 'n element in die transaktiniedgroep, hoe korter is die lewe. Die element met atoomgetal 112 het 'n halfleeftyd van 29 sekondes, 116 - 60 millisekondes, 118 - 0,9 millisekondes. Daar word geglo dat die wetenskap die grense van fisies moontlike materie bereik.
Oganesyan stem egter nie saam nie. Hy stel die standpunt dat hy in die wêreld van superswaar elemente is. "Eiland van stabiliteit". "Die vervaltyd van nuwe elemente is uiters kort, maar as jy neutrone by hul kerne voeg, sal hul leeftyd toeneem," merk sy op. “Die byvoeging van agt neutrone by elemente nommer 110, 111, 112 en selfs 113 verleng hul lewe met 100 XNUMX jaar. een keer".
Vernoem na Oganesyan, die element Oganesson behoort aan die groep transaktiniede en het atoomnommer 118. Dit is die eerste keer in 2002 gesintetiseer deur 'n groep Russiese en Amerikaanse wetenskaplikes van die Joint Institute for Nuclear Research in Dubna. In Desember 2015 is dit erken as een van die vier nuwe elemente deur die IUPAC/IUPAP Joint Working Group ('n groep wat geskep is deur die International Union of Pure and Applied Chemistry en die International Union of Pure and Applied Physics). Die amptelike naamgewing het op 28 November 2016 plaasgevind. Oganesson ma hoogste atoomgetal i grootste atoommassa tussen alle bekende elemente. In 2002-2005 is slegs vier atome van die 294-isotoop ontdek.
Hierdie element behoort tot die 18de groep van die periodieke tabel, d.w.s. edelgasse (synde sy eerste kunsmatige verteenwoordiger), kan dit egter aansienlike reaktiwiteit toon, anders as alle ander edelgasse. In die verlede is gedink dat oganesson 'n gas was onder standaardtoestande, maar huidige voorspellings dui op 'n konstante toestand van aggregasie onder hierdie toestande as gevolg van die relativistiese effekte wat Oganessian genoem het in die onderhoud wat vroeër aangehaal is. In die periodieke tabel is dit in die p-blok, synde die laaste wortel van die sewende periode.
Beide Russiese en Amerikaanse geleerdes het histories verskillende name daarvoor voorgestel. Op die ou end het IUPAC egter besluit om Hovhannisyan se nagedagtenis te eer deur sy groot bydrae tot die ontdekking van die swaarste elemente in die periodieke tabel te erken. Hierdie element is een van twee (langs die seeborg) wat na 'n lewende persoon vernoem is.

